A DPP4-gátló készítmények receptoriális, illetve azon túlmutató hatásai
A DDP4-gátlók klasszikusan a vércukorszint csökkentésére alkalmazott készítmények 2-es típusú diabéteszben. A jól ismert klasszikus mechanizmus szerint ezen antidiabetikumok gátolják a DPP4 enzim aktivitását a plazmában, megakadályozva ezzel a GLP-1 hormon inaktivációját, amely aztán az inzulinelválasztás stimulációját, valamint a glükagonszekréció gátlását eredményezi. A fentiek mellett az experimentális eredmények, illetve a klinikai megfigyelések alapján a DDP4-gátló készítmények kardioprotektív, neuroprotektív és csontanyagacserére gyakorolt pozitív hatásáról is beszámoltak.
A GLP-1 és GIP élettani sajátosságai
A GLP-1 és a GIP az inkretintengely vércukorszint-szabályozás szempontjából legfontosabb hormonjai. A GLP-1-et a bél L-sejtjei, míg a GIP-t a K-sejtek szekretálják. Mindkét esetben a termelődés legfontosabb ingere a táplálék cukor-, zsír- és aminosav-tartalma. Maga az elválasztás pedig az étkezést követően, hozzávetőlegesen 15 perc elteltével kezdődik. A GLP-1 és a GIP legfontosabb hatása a hasnyálmirigy béta-sejtjeire (1):
- a de novo inzulinszintézis fokozása,
- a tárolt inzulin exocitózisának fokozása,
- a glükózszenzorelemek génexpressziójának fokozása,
- az inzulingén expressziójának erősítése,
- a béta-sejt apoptózisának gátlása,
- a béta-sejt neogenezisének serkentése.
Összességében vércukorszinttől függő módon indukálja az inzulin elválasztását, amely a klinikai gyakorlatban azt eredményezi, hogy érdemben nem növeli a hypoglykaemia kialakulásának rizikóját.
A DDP4-gátlás vércukorszint-szabályozást befolyásoló mechanizmusa
Az aktív GLP-1 és a GIP hormonok működését elsősorban a DPP4 enzim szabályozza, amely képes a GLP-1 enzimatikus inaktiválására. A DDP4 enzim egy szerin-proteáz, amely elsősorban az endothelsejtekben expresszálódik, de megtalálható az egész szervezetben. Két típusa közül a szolúbilis enzimatikusan aktív, míg az extracelluláris forma enzimatikusan inaktív, és az intracelluláris jelátviteli folyamatokban vesz részt. A klasszikus mechanizmusa szerint tehát a DPP4-gátlás megakadályozza a GLP-1 inaktivációját, növelve ezzel a keringő GLP-1 koncentrációját, amely aztán fokozza az inzulinszekréciót, gátolja a glükagonelválasztást, valamint a hepatikus glükózprodukciót. Az említett mechanizmus dominánsan a posztprandiális vércukorszint-emelkedést mérsékli, de hatással van az éhomi vércukorszint csökkentésére is.
A DPP4-gátlás kardioprotektív hatása
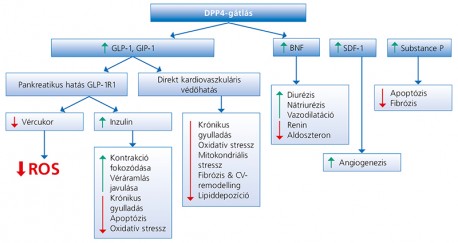
A GLP-1 mellett – amelynek kedvező kardiovaszkuláris hatásai jól ismertek – a DPP4-gátlóknak számos egyéb szubsztrátja is ismert, mint az ANP (atrial natriuretic peptide), a BNP (brain natriuretic peptide), az SDF-1a (stromal cell-derived factor-1a) és a substance P (2, 3). Az ANP a pitvarokban, míg a BNP a kamrákban termelődik. Mindkettő rendelkezik lokális és szisztémás hatással is. Gátolják a renin- és az aldoszteronszekréciót, és fokozzák többek közt a diurézist, a natriurézist és a vazodilatációt (4). Fiziológiásan mindkettő szintje alacsony, de szívelégtelenségben kompenzatorikusan megemelkedik a koncentrációjuk. Az SDF-1a egy kemokin, amely az endotheliális progenitorsejtek „cardiac homing” elősegítése révén stimulálja az angiogenezist, így végül javítja a miokardiális perfúziót. A DDP4-gátlás révén tehát a megtartott SDF-1a-aktívitás eredményeképpen javul a vaszkuláris eseményeket követő helyreállító mechanizmusok hatásfoka. A substance P-nek szerepe van a szívfrekvencia és a vérnyomás szabályozásában, illetve emellett védőhatást mutat az apoptózis, a miokardiális sejtkárosodás, valamint a fibrózis vonatkozásában is (1. ábra) (5).
Összességében tehát elmondható, hogy a részletezett molekuláris mechanizmusok közvetítésével a gliptinek az apoptózis, a krónikus gyulladás, az oxidatív stressz és a vaszkuláris remodelling befolyásolásával lassítják az ateroszklerózist, segítik a miokardiális infarktust követő repair mechanizmusokat.
Glikémiás variabilitás és autonóm neuropátia
A glikémiás variabilitás, azaz a vércukorfluktuáció megítélése a folyamatos szöveti glükózmonitorozó rendszerek (continuous glucose monitoring system, CGMS) széles körű elterjedésével egyre inkább előtérbe került. A fokozott glikémiás variabilitás számos olyan patofiziológiai mechanizmust indukál (oxidatív stressz, poliol-anyagcsereút aktiválása), amelyek fontos szerepet játszanak a szenzoros, valamint az autonóm neuropátia kialakulásában (6). Ráadásul a kardiovaszkuláris autonóm neuropátia (cardiac autonomic neuropathy, CAN) tovább rontja a glikémiás variabilitást, ezáltal mintegy „circulus vitiosus”-t elindítva. A CAN és a hypoglykaemia jól ismert összefüggései mellett egyre több adat bizonyítja a CAN és a glikémiás variabilitás szoros kapcsolatát is, és feltételezik, hogy ebben nemcsak a hypo-, hanem a hyperglykaemiás epizódoknak meghatározó szerepük van (7). Joggal feltételezhetjük tehát, hogy azon antidiabetikumok, amelyek csökkentik a glikémiás variabilitást egyidejűleg kedvezően fogják befolyásolni a CAN-t is. Egy 2022-ben publikált, 14 tanulmány eredményeit áttekintő metaanalízis (8) – amely az MAGE (mean amplitude of glycemic excursios) meghatározáson alapult – igazolta a DPP4-gátlók glikémiás variabilitásra gyakorolt kedvező hatását.
A DPP4-gátlók neuroprotektív hatása
Az utóbbi időkben végzett kutatások alapján a DPP4-gátlók ígéretesnek tűnnek az Alzheimer-kór kialakulásának megelőzésében, illetve a progresszió lassításában (9). A feltételezett patomechanizmus a vércukorkontroll javítása mellett a neuronális inzulinrezisztencia csökkentése és a DPP4-gátlók aß depozitumok képződésére, valamint a tau fehérje hiperfoszforilációjára gyakorolt gátló hatása. Az említettek mellett a DDP-4-gátlók kedvezően befolyásolják számos neuroprotektív szubsztrát (GLP-1, GIP, SDF-1a, NPY) expresszióját és biológiai hasznosulását is. Ugyanakkor mindemellett további klinikai kutatások és randomizált vizsgálatok szükségesek a gyakorlati alkalmazhatóság megítélésének vonatkozásában.
A DPP4-gátlók hatása a csontmetabolizmusra
A DPP4-gátlók csontmetabolizmusra gyakorolt hatása két tengelyen valósul meg (10). Az egyik az ún. entero-endokrin-osszeális, a másik pedig ún. pankreatikus-endokrin-osszeális tengely. Mindkét tengely működésében a DPP4 enzim számos szubsztrátja megtalálható, és a DPP4-gátlás eredményeképpen csökken a csontreszorpció, fokozódik a csontképződés, amely aztán az oszteoporózis csökkenéséhez és a csonttörési kockázat mérséklődéséhez vezet.
Összefoglalás
A DPP4-gátlók tehát a jól ismert vércukorszint-csökkentő hatáson túl számos egyéb, talán pleiotrop hatásként is értelmezhető tulajdonsággal is bírnak. Ezek klinikai relevanciája ma is intenzív kutatások tárgya, de az egyénre szabott antidiabetikumválasztásnál mindenképpen figyelembe veendő tényező. Ezek közül is talán kiemelendő a csonttörések kockázatának csökkentése, hiszen az idős cukorbetegnél ez egy nagyon súlyos és nehezen kezelhető probléma.
A cikk a Sandoz Hungária Kft. felkérésére készült. A cikkben megfogalmazott állítások teljes mértékben a szerző saját véleményét tükrözik. Amennyiben a cikk hatóanyagot említ, mindig az azt tartalmazó termék érvényes alkalmazási előírása az irányadó. RSdz4268/09.2. Lezárás dátuma: 2024. 10. 11.
2. Omar B, Ahrén B. Pleiotropic mechanisms for the glucose-lowering action of DPP-4 inhibitors. Diabetes 2014; 63: 2196–2202.
3. Harangi M, Tóth N, Katona É. A dipeptidyl-peptidáz-4 gátlók szerepe a 2-es típusú diabetes mellitus kezelésében napjainkban. Diabetologia Hungarica 2023; 31(2): 113–122.
4. Nishikimi T, Maeda N, Matsuoka H. The role of natriuretic peptides in cardioprotection. Cardiovasc Res. 2006; 69(2): 318–328.
5. Zakaria M, Tawfeek M, Hassanin M, et al. Cardiovascular protection by DPP‑4 inhibitors in preclinical studies: an updated review of molecular mechanisms. Naunyn-Schmiedeberg's Archives of Pharmacology 2022; 395: 1357–1372.
6. Kempler P, Horváth V. A kardiovaszkuláris kockázat, a DPP-4-gátlók, a vércukor-variabilitás és az autonóm neuropathia potenciális összefüggései. Diabetologia Hungarica 2023; 31(4): 287–293.
7. Gad H, Elgassim E, Mohamed I, et al. Cardiovascular autonomic neuropathy is associated with increased glycemic variability driven by hyperglycemia rather than hypoglycemia in patients with diabetes. Diabetes Res Clin Pract. 2023; 200: 110670.
8. Chai S, Zhang R, Zhang Y, et al. Influence of dipeptidyl peptidase-4 inhibitors on glycemic variability in patients with type 2 diabetes: A meta-analysis of randomized controlled trials. Front Endocrinol. 2022; 13: 935039.
9. Jiang X, Li J, Yao X, et al. Neuroprotectiv effects of dipeptidyl peptidase 4 inhibitor on Alzheimer’s disease: a narrative review. Front Pharmacol. 2024; 15: 1361651.
10. Pechmann LM, Pinheiro FI, Andrade VFC, et al. The multiple actions of dipeptidyl peptidase 4 (DPP-4) and its pharmacological inhibition on bone metabolism: a review. Diabetology & Metabolic Syndrome 2024; 16: 175.
Cikk értékelése
| Eddig 15 felhasználó értékelte a cikket. |


Hozzászólások